Autor:XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
Szkoła Nauki i Inżynierii Materiałowej, Uniwersytet Nauki i Technologii w Nanjing, Nanjing 210094, Chiny
Abstrakcyjny
Całkowicie półprzewodnikowa cienkowarstwowa bateria litowa (TFLB) jest uważana za idealne źródło zasilania urządzeń mikroelektronicznych. Jednakże stosunkowo niska przewodność jonowa amorficznego elektrolitu w stanie stałym ogranicza poprawę parametrów elektrochemicznych TLB. W tej pracy cienkie warstwy amorficznego tlenoazotku litowo-krzemowego (LiSiON) są przygotowywane poprzez rozpylanie magnetronowe jako elektrolit w stanie stałym dla TLB. Dzięki zoptymalizowanym warunkom osadzania cienka warstwa LiSiON wykazuje wysoką przewodność jonową wynoszącą 6,3×10-6 S∙cm-1 w temperaturze pokojowej i szerokie okno napięciowe powyżej 5 V, co czyni go odpowiednim elektrolitem cienkowarstwowym do TLB. MoO3/LiSiON/Li TFLB jest zbudowany w oparciu o cienkowarstwowy elektrolit LiSiON o dużej pojemności właściwej (282 mAh∙g-1 przy 50 mA∙g-1), dobrej wydajności (50 mAh∙g -1 przy 800 mA∙g-1) i akceptowalną trwałość cyklu (78,1% utrzymania pojemności po 200 cyklach), co pokazuje przydatność tego elektrolitu do zastosowań praktycznych.
Słowa kluczowe:LiSiON; elektrolit cienkowarstwowy; całkowicie półprzewodnikowa bateria litowa; bateria cienkowarstwowa
Szybki rozwój przemysłu mikroelektronicznego, takiego jak systemy mikroelektromechaniczne (MEMS), mikroczujniki, inteligentne karty i wszczepialne mikrourządzenia medyczne, prowadzi do rosnącego zapotrzebowania na zintegrowane magazyny energii o rozmiarach mikro[1,2]. Wśród dostępnych technologii akumulatorów, całkowicie półprzewodnikowe cienkowarstwowe akumulatory litowe (TFLB) są uważane za idealne źródło zasilania dla urządzeń mikroelektronicznych ze względu na ich wysokie bezpieczeństwo, niewielkie rozmiary, konstrukcję typu power-on-chip, długą żywotność i niski stopień samorozładowania. Jako jeden z kluczowych składników TLB, cienkowarstwowy elektrolit w stanie stałym odgrywa istotną rolę w określaniu właściwości TLB[3]. Dlatego opracowanie wysokowydajnego cienkowarstwowego elektrolitu w stanie stałym jest zawsze ważnym celem rozwoju TLB. Obecnie najczęściej stosowanym elektrolitem w TFLB jest amorficzny tlenoazotek litu i fosforu (LiPON), który ma umiarkowane przewodnictwo jonowe (2×10-6 S∙cm-1), niskie przewodnictwo elektronowe (~{{5 }} S∙cm-1), szerokie okno napięciowe (~5,5 V) i dobra stabilność styku z litem[4,5]. Jednak jego przewodność jonowa jest stosunkowo niska, co utrudnia przyszły rozwój TFLB dużej mocy na nadchodzącą erę Internetu Rzeczy (IoT)[6]. Dlatego pilnie potrzebne jest opracowanie nowych elektrolitów cienkowarstwowych o zwiększonej przewodności jonowej, a także dużym oknie napięciowym i dobrej stabilności kontaktu z litem dla TLB nowej generacji.
Spośród różnych nieorganicznych materiałów elektrolitów w stanie stałym, układ roztworów stałych Li2O-SiO2 i ich fazy deuterogenne zidentyfikowano jako potencjalne elektrolity cienkowarstwowe ze względu na ich szybkie, trójwymiarowe kanały przewodzące lit[7]. Na przykład Chen i in.[8]podali, że stały elektrolit Li4,4Al0.4Si0.6O4-0.3Li2O podstawiony Al ma wysoką przewodność jonową wynoszącą 5,4×10-3 S∙cm{{12} } w temperaturze 200 stopni . Adnan i in.[9] odkryli, że związek Li4Sn0.02Si0,98O4 ma maksymalną wartość przewodności 3,07×10-5 S∙cm-1 w temperaturze otoczenia. Jednakże poprzednie prace nad układami elektrolitów Li2O-SiO2 skupiały się głównie na materiałach proszkowych o wysokiej krystaliczności, natomiast bardzo ograniczone prace odnotowano nad ich amorficznymi, cienkowarstwowymi odpowiednikami dla TLB. Ponieważ TFLB jest zwykle tworzony poprzez osadzanie cienkich warstw katody, elektrolitu i anody warstwa po warstwie, wymagane jest przygotowanie warstwy elektrolitu w stosunkowo niskiej temperaturze, aby uniknąć niekorzystnych interakcji pomiędzy katodą i elektrolitem, które powodują pęknięcia i zwarcia TLB[1,2]. Zatem opracowanie elektrolitu Li2O-SiO2 o właściwościach amorficznych przygotowanego w niskiej temperaturze jest ważne dla TLB. Chociaż niedawna praca[6] pokazuje, że wysoką przewodność litowo-jonową wynoszącą 2,06×10-5 S∙cm-1 można uzyskać za pomocą cienkiej warstwy amorficznego Li-Si-PON, a jej stabilność kontaktowa z elektrodami i stabilność elektrochemiczna w TLB muszą jeszcze zostać zostać zbadane. Dlatego niezwykle ważne jest opracowanie wysokowydajnego cienkowarstwowego elektrolitu na bazie Li2O-SiO2 i wykazanie jego rzeczywistego zastosowania w TLB.
W tej pracy cienką warstwę amorficznego tlenoazotku litowo-krzemowego (LiSiON) przygotowano metodą rozpylania magnetronowego o częstotliwości radiowej (RF) w temperaturze pokojowej i zbadano ją jako elektrolit w stanie stałym dla TLB. Moc rozpylania i przepływ gazu roboczego N2/Ar zostały zoptymalizowane w celu uzyskania najlepszych warunków osadzania cienkiej warstwy LiSiON. Ponadto, aby wykazać przydatność zoptymalizowanego elektrolitu LiSiON do TLB, skonstruowano pełne ogniwo MoO3/LiSiON/Li i systematycznie badano jego właściwości elektrochemiczne.
1 Eksperymentalny
1.1 Przygotowanie cienkich warstw LiSiON
Cienkie folie LiSiON przygotowano metodą rozpylania magnetronowego RF (Kurt J. Lesker) przy użyciu tarczy Li2SiO3 (o średnicy 76,2 mm) w temperaturze pokojowej przez 12 godzin. Przed osadzaniem ciśnienie w komorze obniżono do mniej niż 1×10-5 Pa. Odległość od celu do podłoża wynosiła 10 cm. Próbki osadzone przy mocy RF 80, 100 i 120 W przy przepływie 90 sccm N2 są oznaczone jako próbki LiSiON-80N9, LiSiON-100N9 i LiSiON-120N9, odpowiednio. Natomiast próbki osadzone przy mocy RF 100 W przy przepływie 90 sccm N2 i 10 sccm Ar, 90 sccm N2 i 50 sccm Ar, 50 sccm N2 i 50 sccm Ar są oznaczone jako próbka LiSiON- 100N9A1, LiSiON Odpowiednio -100N9A5 i LiSiON-100N5A5.
1.2 Przygotowanie MoO3/LiSiON/Li TLB
Zgodnie z naszym poprzednim raportem, folię MoO3 przygotowano metodą reaktywnego rozpylania magnetronowego prądem stałym (DC) (Kurt J. Lesker) przy użyciu tarczy MoO z czystego metalu (o średnicy 76,2 mm).[10]. Odległość tarczy od podłoża wynosiła 10 cm, a moc napylania DC 60 W. Osadzanie przeprowadzono w temperaturze podłoża 100 stopni przez 4 h przy przepływie 40 sccm Ar i 10 sccm O2, metodą wyżarzania in-situ obróbka w temperaturze 450 stopni przez 1 godzinę. LiSiON-100Następnie osadzono N9A1 na warstwie MoO3 jako elektrolit. Następnie na folii LiSiON osadzono metaliczną warstwę litu o grubości około 2 µm poprzez termiczne odparowanie próżniowe (Kurt J. Lesker). Ostatni etap produkcji obejmował osadzanie kolektora prądu Cu i proces hermetyzacji.
1.3 Charakterystyka materiału
Strukturę krystaliczną próbek scharakteryzowano metodą dyfrakcji promieni rentgenowskich (XRD, Bruker D8 Advance). Morfologię i mikrostrukturę próbek scharakteryzowano za pomocą skaningowego mikroskopu elektronowego z emisją polową (FESEM, FEI Quanta 250F) wyposażonego w spektroskopię rentgenowską z dyspersją energii (EDS). Skład pierwiastkowy próbek analizowano metodą spektrometrii masowej w plazmie indukcyjnie sprzężonej (ICP-MS, Agilent 7700X). Skład chemiczny i informacje o wiązaniu próbek mierzono za pomocą rentgenowskiej spektroskopii fotoelektronów (XPS, Escalab 250XI, Thermo Scientific).
1.4 Pomiary elektrochemiczne
Przewodność jonową cienkowarstwowego elektrolitu LiSiON mierzono przy użyciu warstwowej struktury Pt/LiSiON/Pt. Pomiary elektrochemicznej spektroskopii impedancyjnej (EIS) (od 1000 kHz do 0,1 Hz z amplitudą potencjału 5 mV) i woltamperometrii cyklicznej (CV) próbek przeprowadzono na aparacie elektrochemicznym Biologic VMP3 stacja robocza. Pomiar galwanostatycznego ładowania/rozładowania (GCD) MoO3/LiSiON/Li TFLB przeprowadzono przy użyciu układu akumulatorów Neware BTS4000 w komorze rękawicowej wypełnionej argonem w temperaturze pokojowej. Do określenia obciążenia masowego elektrody użyto wagi analitycznej Sartorius (CPA225D, o rozdzielczości 10 ug), a obciążenie masowe warstewki MoO3 wynosi około 0,4 mg∙cm-2.
2 Wyniki i dyskusja
Jak pokazano na obrazie optycznym zamieszczonym na ryc. 1 (a), do przygotowania cienkiej warstwy LiSiON wykorzystano tarczę Li2SiO3. Wynik XRD na rys. 1(a) pokazuje, że target składa się z głównej fazy Li2SiO3 (JCPDS 83-1517) i mniejszej fazy SiO2. Pomiar ICP-MS wskazuje, że stosunek atomowy Li:Si w tarczy wynosi około 1,79:1. Dla typowej próbki LiSiON-100N9A1 po napyleniu tarczy otrzymano przezroczystą, amorficzną cienką warstwę (rys. 1(b)). Grubość typowej próbki LiSiON-100N9A1 zmierzona na obrazie przekroju poprzecznego FESEM na ryc. 1(c) wynosi około 1,2 μm, co wskazuje na szybkość wzrostu około 100 nm∙h-1 poniżej tego stan : schorzenie. Jak pokazano na obrazie FESEM w widoku z góry na ryc. 1 (d), powierzchnia cienkiej warstwy LiSiON jest bardzo gładka i gęsta, bez pęknięć i porów, co czyni go odpowiednim stałym elektrolitem dla TLB, aby uniknąć skrótów i problemów związanych z bezpieczeństwem.
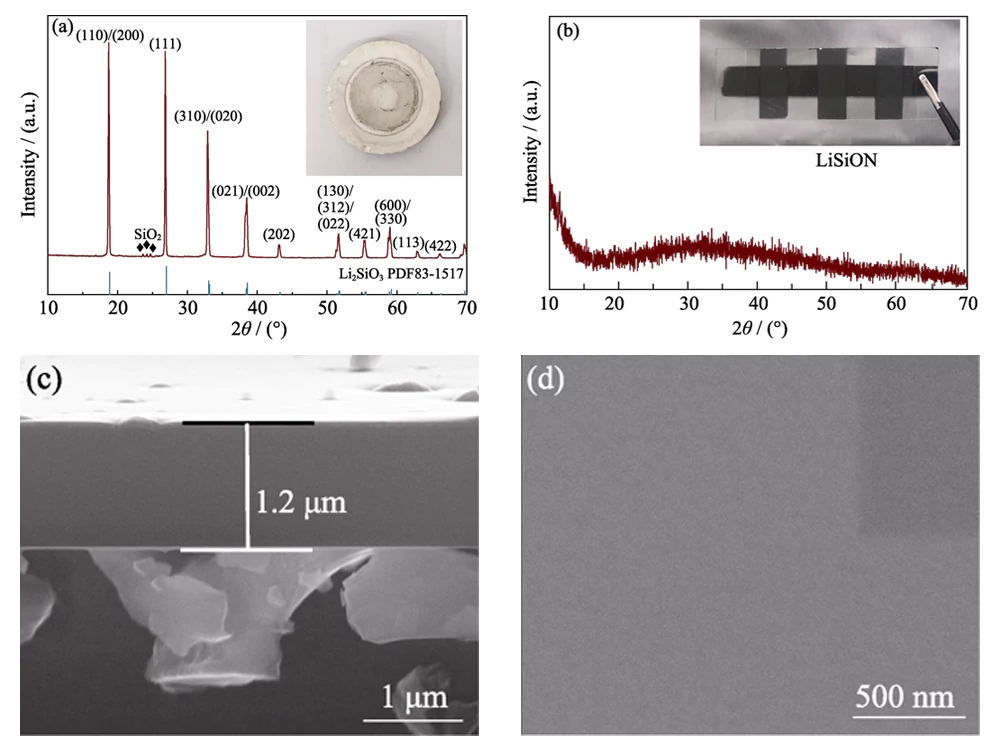
Rys. 1 (a) Wzór XRD i obraz optyczny tarczy Li2SiO3; (b) wzór XRD i obraz optyczny typowej próbki LiSiON- 100N9A1; (c) Przekrój poprzeczny i (d) obrazy FESEM w widoku z góry typowej próbki LiSiON-100N9A1
Analizę XPS przeprowadzono w celu zbadania składu chemicznego i informacji o wiązaniu tarczy Li2SiO3 i typowej próbki LiSiON-100N9A1. Widma skanowania przeglądu XPS na ryc. 2 (a) ujawniają obecność pierwiastków Li, Si i O w tarczy Li2SiO3 oraz wprowadzenie pierwiastka N do cienkiej warstwy LiSiON. Stosunek atomowy N:Si w cienkiej warstwie LiSiON wynosi około 0,33:1, zgodnie z wynikiem XPS. W połączeniu z odpowiednim stosunkiem atomowym (1,51:1) uzyskanym za pomocą pomiaru ICP-MS, stechiometria typowej próbki LiSiON-100N9A1 wynosi Li1.51SiO2.26N0.33. W porównaniu z pojedynczym pikiem Si-Si (103,2 eV) w widmie XPS na poziomie rdzenia Si2p tarczy Li2SiO3 (ryc. 2(b)), dodatkowy pik Si-N (101,6 eV) można zaobserwować z cienkiej warstwy LiSiON , co sugeruje występowanie azotowania w LiSiON[11,12]. Widmo XPS celu Li2SiO3 na poziomie rdzenia O1s na ryc. 2 (c) pokazuje dwa środowiska wiązania: 531,5 eV pochodzące z SiOx i 528,8 eV przypisane do Li2O. Po osadzeniu, za pomocą cienkiej warstwy LiSiON można zaobserwować dodatkowy składnik przy 530,2 eV, który można przypisać niemostkującemu tlenowi (On) w krzemianie[13,14]. Widmo XPS cienkiej warstwy LiSiON na poziomie rdzenia N1 na rys. 2(d) można rozłożyć na trzy piki, w tym 398,2 eV dla wiązania Si-N, 396,4 eV dla Li3N i 403,8 eV dla azotynów NO{{11} }, co dodatkowo potwierdza włączenie N do sieci LiSiON[14,15,16]. Jak schematycznie pokazano na ryc. 2 (e), włączenie N do sieci LiSiON może utworzyć bardziej usieciowaną strukturę, co jest korzystne dla szybkiego przewodzenia jonów litu[6,17].
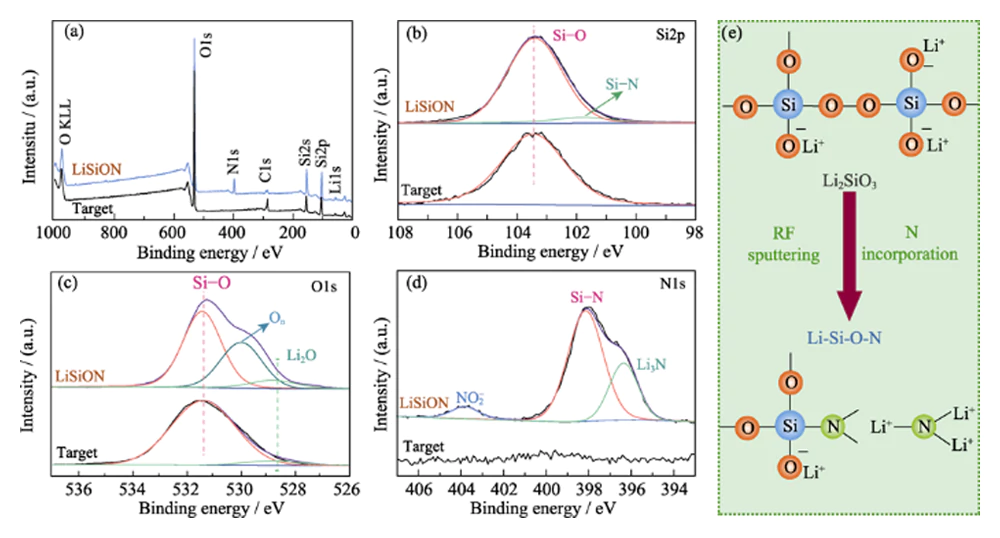
Ryc. 2 (a) Skanowanie pomiarowe, (b) poziom rdzenia Si2p, (c) poziom rdzenia O1s i (d) widma XPS poziomu rdzenia N1s celu Li2SiO3 i typowej próbki LiSiON-100N9A1; (e) Schematyczna ilustracja częściowej zmiany struktury z Li2SiO3 na LiSiON z włączeniem N
Aby zoptymalizować przewodność jonową i stabilność elektrochemiczną cienkich warstw LiSiON, porównano różne cienkie warstwy LiSiON osadzone przy różnych mocach rozpylania i przepływy gazu roboczego pod kątem ich przewodności jonowej i okien napięcia. Wykresy Nyquista w temperaturze pokojowej dla cienkich warstw LiSiON przedstawiono na ryc. 3 (a), a odpowiednią strukturę warstwową Pt/LiSiON/Pt i obwód zastępczy pokazano na ryc. 3 (b). Jak zaobserwowano, wykresy Nyquista wykazują pojedyncze półkole i ogon pojemności dielektrycznej, co jest charakterystyczne dla cienkowarstwowego dielektryka przewodzącego z procesem relaksacji objętościowej umieszczonej pomiędzy stykami blokującymi[17]. Przewodnictwo jonowe (σi) cienkich warstw LiSiON można obliczyć za pomocą równania. (1).
σi=d/(RA)
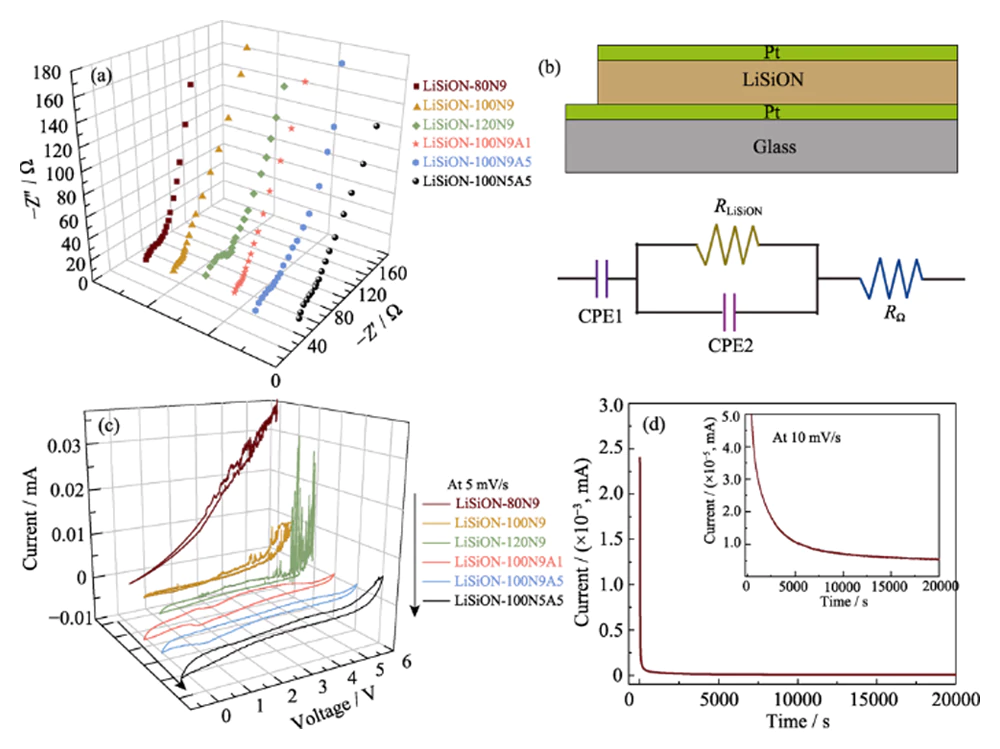
Rys. 3 (a) Widma elektrochemicznej spektroskopii impedancyjnej (EIS) cienkich warstw LiSiON osadzonych w różnych warunkach; (b) Schematyczna ilustracja struktury warstwowej Pt/LiSiON/Pt i odpowiedniego obwodu zastępczego; (c) Krzywe CV cienkich warstw LiSiON osadzonych w różnych warunkach; (d) Krzywa chronoamperometrii próbki LiSiON-100N9A1
gdzie d jest grubością folii, A jest powierzchnią efektywną (około 1 cm2), a R jest rezystancją folii oszacowaną na podstawie zmierzonego wykresu Nyquista. Obliczone przewodności jonowe tych cienkich warstw LiSiON porównano w tabeli 1. Jak zaobserwowano, przewodność jonowa cienkiej warstwy LiSiON osadzonej przy stałym przepływie 90 sccm N2 wzrasta wraz ze wzrostem mocy rozpylania od 80 W do 100 W, a następnie maleje gdy moc rozpylania zostanie dodatkowo zwiększona do 120 W, co jest wartością podobną do poprzedniego raportu na temat elektrolitu LiPON[18]. Wyraźny wzrost przewodności jonowej można zaobserwować, gdy promowany jest stosunek N2 w gazie roboczym przy stałej mocy rozpylania 100 W, co można przypisać zwiększonej ilości azotu wprowadzonego do LiSiON w bardziej sprzyjającym środowisku dla jonów litu ruch[5, 18]. Warto zauważyć, że próbki LiSiON- 100N9 i LiSiON-100N9A1 wykazują najwyższe przewodnictwo jonowe, odpowiednio 7,1×10-6 i 6,3×10-6 S∙cm-1 , które są oczywiście wyższe niż dobrze znany LiPON (~2×10-6 S∙cm-1), wcześniej raportowany amorficzny LiNbO3 (~1×10-6 S∙cm{{19} })[19], LiBON (2,3×10-6 S∙cm-1)[20], Li-V-Si-O (~1×10-6 S∙cm-1)[21], Li-La-Zr-O (4×10-7 S∙cm-1)[22]i Li-Si-PO (1,6×10-6 S∙cm-1)[23]warstw elektrolitów, co ujawniło, że cienka warstwa amorficznego LiSiON jest konkurencyjnym kandydatem na elektrolit do TLB. Wysoką przewodność jonową cienkiej warstwy LiSiON można przypisać włączeniu N do cienkiej warstwy i utworzeniu wiązań Si-N zamiast wiązań Si-O, co prowadzi do bardziej usieciowanej sieci anionowej zapewniającej łatwą mobilność jonów litu[17, 24]. Okna elektrochemicznie stabilnego napięcia cienkich warstw LiSiON oceniano poprzez pomiar CV przy szybkości skanowania 5 mV∙s-1 przy napięciu do 5,5 V. Należy podkreślić, że wpływ warunków osadzania na napięcie okno folii LiSiON jest różne, czego obecnie nie można wytłumaczyć jasnym mechanizmem, ponieważ w poprzednich raportach nie było odpowiednich badań na temat elektrolitu cienkowarstwowego[18,24-25]. Niemniej jednak, w porównaniu na rys. 3(c) i w tabeli 1, próbki LiSiON-100N9A1 i LiSiON- 100N5A5 wykazują najszersze okna napięcia ~5.0 i ~5,2 V , które są zbliżone do elektrolitu LiPON. Dlatego też, biorąc pod uwagę zarówno przewodność jonową, jak i okno napięcia, wybrano próbkę LiSiON- 100N9A1 do dalszych badań i wytworzenia pełnego ogniwa. Aby zbadać liczbę przenoszenia jonów litu (τi) i przewodność elektronową (σe) próbki LiSiON-100N9A1, przeprowadzono dalej chronoamperometrię przy stałym napięciu 10 mV (ryc. 3(d)). τi można obliczyć za pomocą równania. (2).
τi=(Ib-Ie)/Ib
gdzie Ib jest początkowym prądem polaryzacji, a Ie jest prądem stanu ustalonego[18]. Obliczono, że współczynnik τi wynosi 0,998, co jest bliskie 1, co wskazuje, że w elektrolicie zdecydowanie dominuje przewodzenie jonów litu. Współczynnik τi zależy od mieszanego efektu przewodzenia jonów i elektronów[24], co można wyrazić równaniem. (3).
τi=σi/(σi+σe)
Zatem σe próbki LiSiON-100N9A1 oblicza się na 1,26×10-8 S∙cm-1, co jest nieistotne w porównaniu z jej przewodnością jonową.
Tabela 1 Porównanie przewodności jonów litu i okien napięciowych cienkich warstw LiSiON osadzonych w różnych warunkach
|
Próbka |
Przewodność jonów litu |
Napięcie |
|
LiSiON-80N9 |
4.6 |
~2.0 |
|
LiSiON-100N9 |
7.1 |
~3.9 |
|
LiSiON-120N9 |
2.5 |
~4.2 |
|
LiSiON-100N9A1 |
6.3 |
~5.0 |
|
LiSiON-100N9A5 |
3.0 |
~4.6 |
|
LiSiON-100N5A5 |
2.9 |
~5.2 |
Aby zweryfikować wykonalność zoptymalizowanej próbki LiSiON{{0}}N9A1 do zastosowania w TFLB, wyprodukowano MoO3/LiSiON/Li TFLB. Obraz przekroju poprzecznego FESEM i odpowiednie obrazy mapowania EDS MoO3/LiSiON/Li TLB pokazano na ryc. 4 (a). Jak zaobserwowano, katoda MoO3 (o grubości około 1,1 μm) i anoda Li są dobrze oddzielone elektrolitem LiSiON, a elektrolit LiSiON ma ścisłe styki zarówno z katodą, jak i anodą. Ryc. 4(b) przedstawia typową krzywą CV TFLB przy szybkości skanowania 0,1 mV∙s-1 pomiędzy 1,5-3,5 V, co pokazuje parę dobrze zdefiniowanych pików redoks przy napięciu około 2,25 i 2,65 V, co odpowiada wprowadzaniu jonów litu do i ekstrakcji z MoO3[10]. Rys. 4(c) przedstawia początkowe 3 krzywe galwanostatycznego ładowania/rozładowania TLB przy gęstości prądu 50 mA∙g-1 (20 μA∙cm-2, w oparciu o masę warstwy MoO3 ). Jak zaobserwowano, TFLB zapewnia początkową pojemność ładowania/rozładowania wynoszącą 145/297 mAh∙g-1 (58/118,8 μAh∙cm-2). Po drugim cyklu TLB uzyskał stabilną pracę cykliczną z wysoką odwracalną pojemnością właściwą wynoszącą 282 mAh∙g-1. Wydajność szybkościową TFLB przy różnych gęstościach prądu przedstawiono na ryc. 4 (d). Nieodwracalną utratę pojemności TFLB w pierwszych kilku cyklach przy niskiej gęstości prądu można przypisać nieodwracalnemu przejściu fazowemu w MoO3 uzyskanym przez wprowadzenie litu[26]. Stabilne pojemności rozładowania wynoszące około 219, 173, 107 i 50 mAh∙g-1 są obserwowane odpowiednio przy 100, 200, 400 i 800 mA∙g-1, co świadczy o dobrej wydajności. Aby ocenić stabilność elektrochemiczną TFLB, przeprowadzono dalsze cykle przy gęstości prądu 200 mA∙g-1 (ryc. 4(e)). TLFB może zachować 78,1% swojej początkowej pojemności rozładowania po 200 cyklach, a wydajność kulombowska wynosi prawie 100% w każdym cyklu, co wskazuje na akceptowalną stabilność elektrochemiczną elektrolitu LiSiON. Pomiary EIS przeprowadzono dalej przy napięciu obwodu otwartego, aby zbadać granicę faz elektrolit/elektroda w TLB przy różnych liczbach cykli, a odpowiednie wykresy Nyquista z obwodem równoważnym przedstawiono na rys. 4 (f). Jak zaobserwowano, MoO3/LiSiON/Li TFLB wykazuje podobne widmo EIS, które składa się z dwóch półkoli w obszarze wysokich częstotliwości w stanie świeżym, do widma MoO3/LiPON/Li TFLB w naszej poprzedniej pracy[10], co wskazuje, że rezystancja międzyfazowa Li/LiSiON jest znikoma w porównaniu z rezystancją interfejsu LiSiON/MoO3[20]. Pierwsze małe półkole na wykresach Nyquista przypisuje się przewodzeniu jonowemu jonów Li+ w elektrolicie LiSiON, natomiast drugie duże półkole odpowiada procesowi przenoszenia ładunku na granicy faz LiSiON/MoO3[27,28]. Należy zauważyć, że pierwsze małe półkole rzadko zmienia się podczas cykli, co wskazuje na stosunkowo dobrą stabilność cykliczną elektrolitu LiSiON. Jednakże drugie półkole stopniowo się rozszerza wraz ze zmianą liczby cykli, ujawniając zwiększoną rezystancję międzyfazową LiSiON/MoO3 podczas pracy cyklicznej, co może być główną przyczyną spadku pojemności TFLB[29]. Warto wspomnieć, że w tej pracy z powodzeniem zastosowano elektrolit LiSiON do budowy TFLB i po raz pierwszy wykazano dobry kontakt międzyfazowy LiSiON zarówno z katodą MoO3, jak i anodą litową. Co więcej, duża pojemność właściwa, dobra wydajność i akceptowalna wydajność cyklu MoO3/LiSiON/Li TFLB pokazują, że cienka warstwa LiSiON dobrze nadaje się jako elektrolit do TFLB.
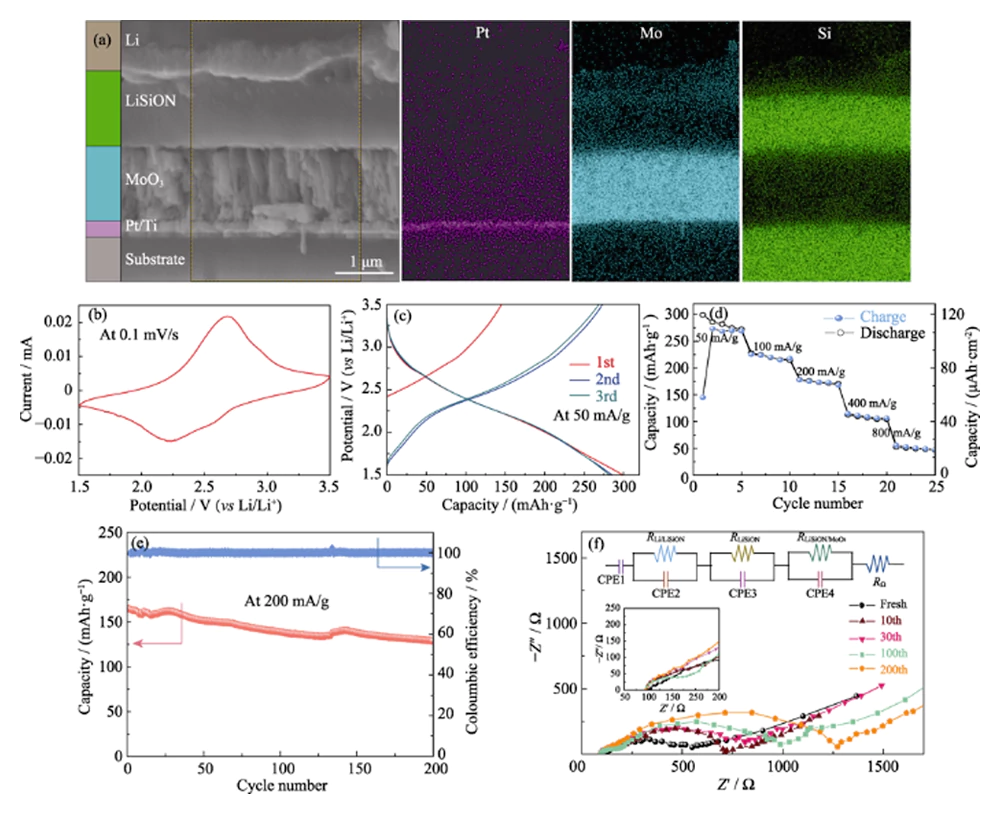
Ryc. 4 (a) Przekrój poprzeczny obrazu FESEM i odpowiadające mu obrazy mapowania EDS MoO3/LiSiON/Li TLBB; (b) Typowa krzywa CV, (c) początkowe trzy krzywe ładowania/rozładowania, (d) wydajność szybkości, (e) wydajność cyklu oraz (f) widma EIS przy różnych numerach cykli MoO3/LiSiON/Li TFLB z próbką LiSiON -100N9A1 jako elektrolit
3 Wnioski
Podsumowując, amorficzny cienkowarstwowy elektrolit LiSiON został pomyślnie przygotowany za pomocą rozpylania magnetronowego RF przy użyciu tarczy Li2SiO3 w przepływie gazu N2/Ar. Zoptymalizowana cienka warstwa LiSiON osadzona przy mocy RF 100 W przy przepływie 90 sccm N2 i 10 sccm Ar charakteryzuje się gładką powierzchnią, gęstą strukturą i wysoką przewodnością jonową (6,3×10-6 S∙cm-1) i szerokie okno napięcia (5 V), co czyni go obiecującym materiałem elektrolitowym dla TLB. Co ważniejsze, dzięki zastosowaniu elektrolitu LiSiON po raz pierwszy pomyślnie zademonstrowano MoO3/LiSiON/Li TFLB o dużej pojemności właściwej (282 mAh∙g-1 przy 50 mA∙g-1), dobrej wydajność prądową (50 mAh∙g-1 przy 800 mA∙g-1) i akceptowalną stabilność cykli (utrzymanie pojemności na poziomie 78,1% po 200 cyklach). Oczekuje się, że prace te przyniosą nowe możliwości opracowania wysokowydajnego TFLB przy użyciu cienkowarstwowego elektrolitu na bazie Li2O-SiO2.
Bibliografia
[1] MOITZHEIM S, PUT B, VEREECKEN P M. Postępy w cienkowarstwowych bateriach litowo-jonowych 3D. Zaawansowane interfejsy materiałowe, 2019, 6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S i in. Przerost tunelowy Układy nanoarkuszów LixMnO2 jako katoda 3D dla wysokowydajnych, cienkowarstwowych mikrobaterii litowych o dużej wydajności, w całości półprzewodnikowych. Materiały zaawansowane, 2021, 33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B i in. Zwiększanie przewodności jonów litu w stałych elektrolitach litowo-jonowych (LISICON) poprzez efekt mieszanego polianionu. Materiały i interfejsy stosowane ACS, 2017, 9(8):7050-7058.
[4] BATES JB, DUDNEY NJ, GRUZALSKI GR i in. Wytwarzanie i charakterystyka cienkich warstw amorficznego elektrolitu litowego i akumulatorów cienkowarstwowych. Journal of Power Sources, 1993, 43(1/2/3):103-110.
[5] BATES J. Właściwości elektryczne cienkich warstw amorficznego elektrolitu litowego. Solid State Ionics, 1992, 53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O i in. Zależność składu przewodnictwa jonowego w cienkowarstwowych elektrolitach LiSiPO(N) do akumulatorów półprzewodnikowych. ACS Applied Energy Materials, 2019, 2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD JN i in. Strukturalne i mechanistyczne spojrzenie na szybkie przewodnictwo litowo-jonowe w elektrolitach stałych Li4SiO4- Li3PO4. Dziennik Amerykańskiego Towarzystwa Chemicznego, 2015, 137(28):9136-9145.
[8] CHEN R, SONG X. Przewodność jonowa stałych elektrolitów dla układów Li4+xMxSi1-xO4-yLi2O (M=Al, B). Dziennik Chińskiego Towarzystwa Chemicznego, 2002, 49:7-10.
[9] ADNAN S, MOHAMED N S. Wpływ podstawienia Sn na właściwości elektrolitu ceramicznego Li4SiO4. Solid State Ionics, 2014,262:559-562.
[10] SUN S, XIA Q, LIU J i in. Samodzielne układy nanopłatków -MoO3-x z niedoborem tlenu jako katoda 3D dla zaawansowanych, całkowicie półprzewodnikowych, cienkowarstwowych akumulatorów litowych. Journal of Materiomics, 2019, 5(2):229-236.
[11] DING W, LU W, DENG X i in. Badanie XPS struktury warstwy SiNx osadzonej metodą mikrofalowego rozpylania magnetronowego ECR. Acta Physica Sinica, 2009, 58(6):4109-4116.
[12] KIM H, KIM Y. Częściowe azotowanie Li4SiO4 i przewodnictwo jonowe Li4. 1SiO3. 9N0. 1Ceramics International, 2018, 44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O i in. Analiza anod SiO do akumulatorów litowo-jonowych. Journal of The Electrochemical Society, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S i in. Reakcja i tworzenie warstwy ładunku przestrzennego na interfejsie LiCoO2-LiPON: spostrzeżenia na temat powstawania defektów i wyrównania poziomów energii jonów dzięki połączonemu podejściu do nauki o powierzchni i symulacji. Materiały chemiczne, 2017, 29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S i in. Redukcja oporu przenoszenia ładunku na granicy faz stały elektrolit-elektroda poprzez pulsacyjne laserowe osadzanie warstw ze źródła krystalicznego Li2PO2N. Journal of Power Sources, 2016, 312:116-122.
[16] SICOLO S, FINGERLE M, HAUSBRAND R i in. Niestabilność międzyfazowa amorficznego LiPON w stosunku do litu: połączona teoria funkcjonału gęstości i badanie spektroskopowe. Journal of Power Sources, 2017, 354:124-133.
[17] WU F, LIU Y, CHEN R i in. Przygotowanie i wykonanie nowatorskiego cienkowarstwowego elektrolitu Li-Ti-Si-PON do cienkowarstwowych akumulatorów litowych. Journal of Power Sources, 2009, 189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J i in. Charakterystyka elektryczna ultracienkich warstw LiPON napylanych metodą RF do akumulatorów w skali nano. Materiały stosowane i interfejsy ACS, 2016, 8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Przewodnictwo Li+ w warstwach Li-Nb-O osadzanych metodą zol-żel. Solid State Ionics, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. Wysokowydajne, elastyczne mikrobaterie półprzewodnikowe oparte na stałym elektrolicie tlenoazotku litu i boru. Journal of Power Sources, 2016, 328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Bateria półprzewodnikowa z cienką warstwą stałego elektrolitu Li2O-V2O5-SiO2. Solid State Ionics, 1990,40-41:964-966.
[22] Kalita D, Lee S, Lee K i in. Właściwości przewodnictwa jonowego amorficznego stałego elektrolitu Li-La-Zr-O do akumulatorów cienkowarstwowych. Solid State Ionics, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A i in. Przygotowanie cienkich warstw amorficznego Li4SiO4-Li3PO4 za pomocą impulsowego osadzania laserowego do wtórnych akumulatorów litowych w całości w stanie stałym. Solid State Ionics, 2011,182:59-63.
[24] TAN G, WU F, LI L i in. Preparat przez rozpylanie magnetronowe cienkowarstwowych elektrolitów na bazie litu, glinu i fosforanu tytanu z dodatkiem azotu do całkowicie półprzewodnikowych akumulatorów litowo-jonowych. The Journal of Physical Chemistry C, 2012, 116(5):3817-3826.
[25] YU X, BATES JB, JELLISON G i in. Stabilny cienkowarstwowy elektrolit litowy: tlenoazotek litowo-fosforowy. Journal of The Electrochemical Society, 1997, 144(2):524.
[26] KIM H, COOK J, LIN H i in. Wakaty tlenowe poprawiają właściwości MoO3-x w zakresie pseudopojemnościowego przechowywania ładunku. Materiały przyrodnicze, 2017, 16:454-460.
[27] SONG H, WANG S, SONG X i in. Całkowicie półprzewodnikowe akumulatory litowo-powietrzne zasilane energią słoneczną, działające w ekstremalnie niskich temperaturach. Nauka o energii i środowisku, 2020, 13(4):1205-1211.
[28] WANG Z, LEE J, XIN H i in. Wpływ warstwy międzyfazowej elektrolitu katodowego (CEI) na długoterminową pracę cykliczną całkowicie półprzewodnikowych akumulatorów cienkowarstwowych. Journal of Power Sources, 2016, 324:342-348.
[29] QIAO Y, DENG H, HE P i in. Ogniwo litowo-metalowe o wydajności 500 Wh/kg oparte na anionowym procesie redoks. Dżul, 2020, 4(6):1311-1323.





